![]() Grant Tan, Kin Ken Chew and Andrew Yersin, Kemin Animal Nutrition and Health
Grant Tan, Kin Ken Chew and Andrew Yersin, Kemin Animal Nutrition and Health
Giới thiệu
Dịch tả heo Châu Phi (ASF) là bệnh do virus gây xuất huyết tràn lan nhanh, có tính truyền nhiễm cao, đe dọa heo nội địa và heo rừng với tỷ lệ chết lên tới 100%1. ASF nhiễm ở châu Á lần đầu tiên được phát hiện ở Trung Quốc với trường hợp đầu tiên được xác nhận là ở tỉnh Liêu Ninh vào đầu tháng 8 năm 20182. Kể từ đó, ASF đã nhanh chóng lây lan sang các tỉnh khác ở Trung Quốc cũng như các nước khác. Đến cuối tháng 9 năm 2019, 11 nước ở Châu Á đã báo cáo nổ dịch ASF cụ thể như: Trung Quốc, Mongolia, Việt Nam, Campuchia, Lào, Myanmar, Philippines, Hong Kong, Hàn Quốc, Triều Tiên và Đông Timor 2.
Thức ăn chăn nuôi đã được báo cáo là một trong những yếu tố nguy cơ chính của việc lây truyền virus ASF (ASFV). Các nghiên cứu tại Đại học Bang Kansas đã phát hiện ra rằng ASF có thể dễ dàng lây truyền bằng đường miệng qua thức ăn bị vấy nhiễm3. Xác suất lây nhiễm ASFV ở heo tăng lên khi mức độ nhiễm (liều lượng) ASFV trong thức ăn tăng lên, và quan trọng hơn là phơi nhiễm nhiều lần3 (Dee và cộng sự) đã chứng minh rằng ASFV có thể tồn tại trong điều kiện vận chuyển xuyên biên giới trong một số nguyên liệu thức ăn chăn nuôi, bao gồm bã nành (SBM) và thức ăn hỗn hợp4. Các nghiên cứu khác cho thấy ASFV có thể tồn tại đến 78 ngày sau ngày sản xuất và đóng bao hoặc niêm phong một số thành phần thức ăn chăn nuôi, ví dụ: axit amin cũng như hỗn hợp vitamin và khoáng chất5. Virus này cũng có thể tồn tại đến 286 ngày trong bã nành6.
Sal CURB® – dựa trên thành phần Formaldehyde đã được báo cáo cho thấy hoạt động chống lại vi rút gây dịch tiêu chảy cấp ở heo (PEDV) trong thức ăn chăn nuôi 7. Formalin ở mức 0,3% cũng đã được chỉ định trong Tạp chí Khoa học của Cơ quan An toàn Thực phẩm Châu Âu (EFSA) về Bệnh Dịch tả heo Châu Phi, có thể vô hiệu hóa ASFV trong 30 phút8. Trong nghiên cứu chi tiết dưới đây, KEMIN đã phối hợp với Viện Nghiên cứu Thú y Quốc gia (NIVR) Việt Nam, để xác định đặc điểm của ASFV được phân lập từ heo bị nhiễm bệnh ở Việt Nam, và kiểm tra sự hoạt động khác biệt của formaldehyde và không chứa formaldehyde của các sản phẩm thương hiệu Sal CURB® của Kemin chống lại ASFV trong thức ăn9.
Từ khóa
Sal CURB® RM E Liquid, Sal CURB® F2 Dry, Sal CURB® K2 Liquid, African Swine Fever, ASF virus, Feed, Swine
Nguyên liệu và phương pháp
Phân lập, định tính và định lượng virus ASF
Virus ASF, VN/Pig/HN/19, đã được phân lập từ mô lách của một con heo bị bệnh từ một trang trại ở Hà Nam, Việt Nam.
ASFV thu hoạch từ mô lách được phân lập bằng nuôi cấy trên đại thực bào phế nang (PAM) của heo. Phân lập ASFV (tức là VN/Pig/HN/19) được xác định bằng PCR giải trình tự của gen B646L, mã hóa cho p72 capsid protein10. Virus VN/Pig/HN/19 được chuẩn bị bằng cách sử dụng tế bào PAM để nuôi cấy. Để chuẩn độ virus, hai phương pháp định lượng bao gồm phản ứng chuỗi polymerase thời gian thực (qPCR) và haemadsorption 50 (HAD50) được sử dụng theo hướng dẫn của OIE11. Trong qPCR, giá trị Cq cao hơn là dấu hiệu của ít vật chất di truyền hơn, và thấp hơn là dấu hiệu của nhiều vật chất di truyền hơn. Mặt khác, với xét nghiệm HAD, điểm số thấp hơn cho thấy sự hiện diện của vật chất virus giảm, trong khi điểm số cao hơn cho thấy sự hiện diện của vật chất virus nhiều hơn.
Thiết kế thí nghiệm để đánh giá hiệu quả của sản phẩm Sal CURB® chống lại ASFV trong thức ăn chăn nuôi.
Năm nhóm đã được nghiên cứu trong nghiên cứu này:
- Đối chứng âm – Cám không gây nhiễm, không xử lý
- Đối chứng dương – Thức ăn gây nhiễm ASFV
- Thử nghiệm 1 – Thức ăn được xử lý bằng Sal CURB® RM E Liquid (33% formaldehyde) ở 3.0 kg / tấn và bị nhiễm ASFV
- Thử nghiệm 2 – Thức ăn được xử lý bằng Sal CURB® RM F2 Dry (4% formaldehyde) ở 3.0 kg / tấn và bị nhiễm ASFV
- Thử nghiệm 3 – Thức ăn được xử lý bằng Sal CURB® K2 Liquid (64% axit hữu cơ, chủ yếu là axit formic) ở 3.0kg / tấn và bị nhiễm ASFV
Sự gây nhiễm ASFV trong thức ăn cho heo là 1 x 105 (HAD50) theo một phương pháp được mô tả bởi Dee và cộng sự4.
Tất cả các mẫu được ủ ở 20˚C và 60% RH trong 7 ngày. Virus được phục hồi từ các mẫu ở ngày 1, 3 và 7 ngày sau khi điều trị (được chỉ định lần lượt là D1, D3 và D7). Lượng vật chất di truyền và hiệu giá virus trong các mẫu được định lượng bằng cách sử dụng các xét nghiệm qPCR và HAD tương ứng.
Kết quả và thảo luận
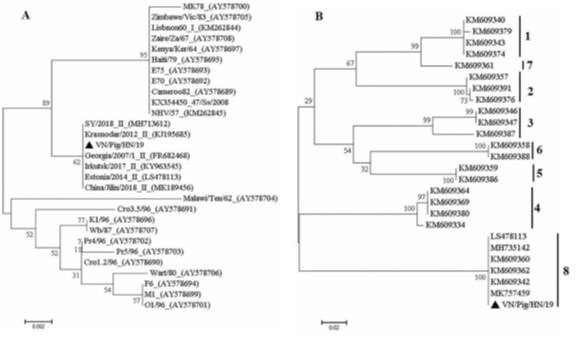
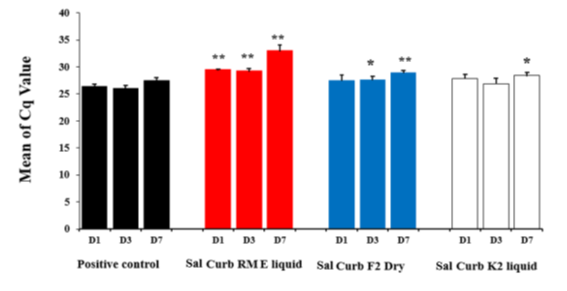
Chủng virus ASF (VN/Pig/HN/19) đã được phân lập thành công từ những con heo bị nhiễm bệnh từ một trang trại ở Việt Nam trong đợt bùng phát ASF vào đầu năm 2019. VN/Pig/HN/19 được phân loại vào nhóm kiểu gen II (Hình 1A) và thuộc kiểu huyết thanh 8 (Hình 1B). Nó có chung 100% nhận dạng nucleotide với các chủng Georgia 2007/1, Krasnodar 2012, Irkutsk 2017, Estonia 2014 và ASFV ‐ SY18 được phân lập ở Georgia, Nga, Estonia và Trung Quốc (Hình 1A). Điều này cho thấy sự bùng phát ASF ở Việt Nam có thể do cùng một chủng ASFV đã được tìm thấy ở Georgia, Estonia và Trung Quốc.Khi VN/Pig/HN/19 được bổ sung vào thức ăn mà không qua bất kỳ xử lý nào, lượng vật chất di truyền và hiệu giá virus vẫn không đổi trong suốt thời gian thí nghiệm (đối chứng dương tính trong Hình 2 và 3). Phát hiện này phù hợp với nghiên cứu trước đây cho thấy ASFV có thể tồn tại trong một thời gian dài trong thức ăn chăn nuôi và vẫn có khả năng lây nhiễm sang heo4. Ngược lại, xử lý thức ăn bằng các sản phẩm Sal CURB® cho thấy mức độ khác nhau của vật chất di truyền và sự ức chế hiệu giá virus (Hình 2 và 3). Sal CURB® RM E Liquid chứa 33% formaldehyde cho thấy hoạt động chống lại ASFV nhiều nhất trong thức ăn chăn nuôi. Giá trị Cq tăng đáng kể từ mức trung bình 26,4 chu kỳ (D1, đối chứng dương) lên 29,5 chu kỳ trên D1 (P <0,01), lên 29,3 chu kỳ trên D3 (P <0,01), lên 33,0 chu kỳ trên D7 (P <0,01) (Hình 2; Sal CURB® RM E Liquid). Sal CURB® F2 Dry chứa axit hữu cơ và 4% formaldehyde cho thấy hoạt tính kém hơn với giá trị Cq lần lượt là 27,7 và 28,9 trên D3 (P <0,05) và D7 (P <0,01), tương ứng. Không chứa formaldehyde, gốc axit hữu cơ Sal CURB® K2 Liquid có hiệu quả thấp nhất với giá trị Cq của 28,4 chu kỳ đạt được trên D7 (P <0,05).
Hình 1. Phân tích phát sinh loài của các chủng ASFV phân lập VN/Pig/HN/19. (A) Phân loại kiểu gen của ASFV. (B) Phân loại huyết thanh của ASFV kiểu gen II.
Hình 2. Chuẩn độ vật liệu di truyền ASFV VN/Pig/HN/19 trong thức ăn bằng cách sử dụng phương pháp real-time PCR vào ngày 1 (D1), 3 (D3) và 7 (D7) sau khi nhiễm virus; Giá trị Cq có nghĩa là ± SEM (n = 3); * P <0,05, ** P <0,01.
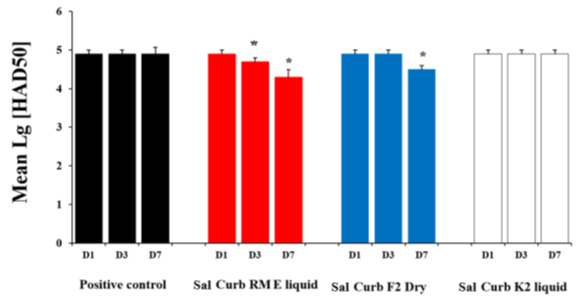
Mặc dù xét nghiệm qPCR có độ nhạy cao và đặc hiệu, nó chỉ đo sự hiện diện của vật liệu di truyền. Để bổ sung cho các nghiên cứu qPCR, xét nghiệm HAD đặc hiệu ASFV đã được sử dụng để đánh giá hiệu giá virus trong thức ăn đã được xử lý. Phù hợp với kết quả qPCR (Hình 2), xét nghiệm HAD cũng cho thấy Sal CURB® RM E Liquid có hoạt tính chống lại ASFV lớn nhất, tiếp theo là Sal CURB® F2 Dry (Hình 3). Sal CURB® RM E Liquid làm giảm hoạt động của virus trong thức ăn trên D3 (P <0,05) và D7 (P <0,05), trong khi Sal CURB® F2 Dry chỉ làm giảm hoạt động của virus trên D7 (P <0,05). Sal CURB® K2 Liquid không có hoạt tính chống lại ASFV. Những kết quả này cho thấy ASFV có thể vẫn lây nhiễm (Hình 3) mặc dù tổng số vật chất di truyền đã giảm đáng kể (Hình 2). Do đó tầm quan trọng của việc sử dụng cả xét nghiệm qPCR và HAD để đánh giá các sản phẩm khác nhau chống lại ASFV.
Hình 3. Chuẩn độ hiệu giá virus ASFV VN/Pig/HN/19 trong thức ăn bằng xét nghiệm HAD vào ngày 1 (D1), 3 (D3) và 7 (D7) sau khi nhiễm virus; log10 giá trị HAD50 là trung bình ± SEM (n = 3); * P <0,05.
Kết luận
1. ASFV được phân lập thành công từ các mẫu ở trang trại.
2. VN/Pig/HN/19 được xác định là thuộc nhóm kiểu gen II và có chung 100% nhận dạng nucleotide với các chủng sau: Georgia 2007/1, Krasnodar 2012, Irkutsk 2017, Estonia 2014 và ASFV ‐ SY18 được phân lập ở Georgia, Nga, Estonia và Trung Quốc.
3. ASFV nuôi cấy trong đại thực bào phế nang heo sống sót trong thức ăn trong thời gian 7 ngày được sử dụng trong nghiên cứu này.
4. Các sản phẩm của Sal CURB® đã chứng minh các hoạt động khác nhau chống lại ASFV trong thức ăn chăn nuôi, như:
5. Sal CURB® RM E Liquid cho thấy hoạt động đáng kể chống lại ASFV (real-time PCR D1, D3 và D7, và HAD trên D3 và D7);
6. Sal CURB® F2 Dry cho thấy hoạt động đáng kể chống lại ASFV (real-time PCR trên D3 và D7 và trên D7 bằng HAD);
7. Sal CURB® K2 Liquid cho thấy ảnh hưởng đáng kể trên D7 bằng real-time PCR. Không có ảnh hưởng nào được quan sát bởi HAD.
Tài liệu tham khảo
- Food and Agriculture Organization of the United Nations 2019. African Swine Fever: A viral disease with 100% fatality rate.
http://www.fao.org/myanmar/news/detail-events/en/c/1177347/
2. Food and Agriculture Organization of the United Nations 2019. ASF situation in Asia Update. http://www.fao.org/ag/againfo/programmes/en/empres/ASF/situation_update.html
3. Niederwerder, M.C., Stoian, A.M.M., Rowland, R.R.R., Dritz, S.S., Petrovan, V., Constance, L.A. Gebhardt, J.T., Olcha, M., Jones, C.K., Woodworth, J.C., Fang, Y., Liang, J., Hefley, T.J. 2019.
Infectious Dose of African Swine Fever Virus When Consumed Naturally in Liquid or Feed. Emerging Infectious Diseases 25(5):891.
4. Dee, S.A., Bauermann, F.V., Niederwerder, M.C., Singrey, A., Clement, T., de Lima, M., Long, C., Patterson, G., Sheahan, M.A., Stoian, A.M.M., Petrovan, V., Jones, C.K., De Jong, J., Spronk, G.D., Minion, L., Christopher-Hennings, J., Zimmerman, J.J., Rowland, R.R.R., Nelson, E., Sundberg, P., Deil, D.G. 2018. Survival of viral pathogens in animal feed ingredients under transboundary shipping models. PLoS ONE 13(3): e0194509.
5. Swine Health Information Center. 2018. Holding Time Calculation for Feed Ingredients.
https://www.swinehealth.org/wp-content/uploads/2018/10/Holding-Time-Calculation-for-Feed-Ingredients.pdf
6. Perrett, M. 2018. US Pork Producers Advised Over Feed Ingredients Amid Swine Fever Outbreak.
https://www.globalmeatnews.com/Article/2018/10/11/US-pork-producers-given-feed-ingredient-advice
7. Dee, S.A., Neil, C., Christopher-Hennings, J., Nelson, E. 2014. An evaluation of a liquid antimicrobial (SalCURB®) for reducing the risk of porcine epidemic diarrhea virus infection of naïve pigs during consumption of contaminated feed. BMC Veterinary Research 10:220.
8. European Food Safety Authority (EFSA) 2010. Scientific Opinion on African Swine Fever. EFSA Journal 8(3):1556.
9. KEMIN internal reference: EPRE-19-1072
10. Garcia-Escudero, R., Andres, G., Almazan, F., Vinuela, E. 1998. Inducible Gene Expression from African Swine Fever Virus Recombinants: Analysis of the Major Capsid Protein p72. Journal of Virology 72(4): 3185.
11. The World Organization for Animal Health (OIE) 2019. Diagnostic tests.
https://www.oie.int/scientific-expertise/veterinary-products/diagnostic-tests/
Dịch bởi: Tịnh Nguyễn, DVM





 In bài viết
In bài viết